أضف إلى السلة
ردمك 978-5-9704-3974-6
الناشر :
"GEOTAR-Media"
عام النشر : 2017
إلى عدد الصفحات: 960
الطبعة: لكل. من الانجليزية.
التنسيق: في الممر.
السعر: 5800 فرك.
المبادئ التوجيهية الأوروبية لأمراض القلب في حالات الطوارئ هي الدليل الرسمي الذي أعدته جمعية رعاية القلب والأوعية الدموية الحادة (ACCA). يوفر الدليل معلومات شاملة عن جميع جوانب الرعاية القلبية المركزة والطارئة.
يناقش الكتاب مختلف أمراض القلب والأوعية الدموية الحادة التي تتطلب رعاية طارئة متخصصة ، فضلاً عن القضايا التنظيمية والتعاون بين مختلف المتخصصين واتباع نهج متعدد التخصصات.
الدليل موجه لجميع المهنيين في مجال الرعاية القلبية المركزة والطارئة: أطباء القلب وجراحو القلب والأوعية الدموية وأخصائيي الإنعاش وأطباء الطوارئ وغيرهم من المهنيين الطبيين.
الفصل الأول. العناية المركزة والطارئة في أمراض القلب: مقدمة
سوزان برايس ، ماركو توبارو ، باسكال فرانكس ، كريستيان رينتس
الفصل 2 التدريب والشهادة في رعاية القلب في حالات الطوارئ
ماجدة هيس ، أليساندرو سيونيس ، سوزان برايس
الفصل 3 سلامة المريض والإرشاد السريري
إليزابيث هكسبي ، سوزان ووكر
الفصل 4. قواعد البيانات والسجلات وجودة الرعاية
نيكولا دانتشين ، فيونا إكارنوت ، فرانسوا شييل
الجزء 1 أقسام ما قبل المستشفى والطوارئ
الفصل 5. الموت القلبي المفاجئ: علم الأوبئة والوقاية
هانز ريتشارد ارنز
الفصل 6
جيري ب.نولان
الفصل 7
مارك ساب ، كوهين برونزيلر ،
أوليفر هوجمارتنز
الفصل 8
إريك دوراند ، أوراس شايب ، ونيكولاس دانشين
الفصل 9
كريستيان مولر
الجزء 2 وحدة العناية المركزة للقلب
الفصل 10
أمراض القلب الطارئة
مناحيم ناهر ، دورون زاجر ، جوناثان حسين
الفصل 11
توم كوين ، إيفا سوان
الفصل الثاني عشر
يساعد
آري بيتر كابيتين ، ستيفان وينديكر
الفصل 13 القضايا الأخلاقية في السكتة القلبية والرعاية القلبية الطارئة: منظور أوروبي
جان لويس فنسنت
الجزء 3 إجراءات المراقبة والتشخيص في وحدة العناية المركزة للقلب
الفصل 14. الفيزيولوجيا المرضية والتقييم السريري لجهاز القلب والأوعية الدموية (بما في ذلك قسطرة الشريان الرئوي)
رومين بارتليمي ، اتيان جيات ، الكسندر مبازة
الفصل الخامس عشر
أنطوان فييار بارون
الفصل السادس عشر
علم الأمراض
كاثي دي داني وجو دينس
الفصل السابع عشر
كارل فيردان ، بريدجز باتيل ، ماتياس جيرندت ، جينينج إبيلت ، يوهان شرودر ، سيباستيان نيودنج
الفصل الثامن عشر
ريتشارد بول ، بافلوس ميريانتيفس ، جورج بالتوبولوس ، شون ماكماستر
الفصل التاسع عشر
الكسندر باركومينكو ، أولغا س. جوريفا ، تاتيانا يالينسكا
الفصل 20
فرانك أ. فلاككامبف ، بافلوس ميريانتيفس ، راكساندرا باير
الفصل 21
ريتشارد بول
الفصل 22
ميشيل إيه دي جراف ، آرثر جيه إتش إيه شولت ، لوسيا كروفت ، جيروين جيه باكس
الفصل 23
يورغ شفيتر ، ينس بريميريتش
إجراءات الجزء 4 في وحدة العناية المركزة للقلب
الفصل 24
جيان أبويلا وأندرو رودس
الفصل 25
جوزيب ماسيب ، كينيث بلاناس ،أرانتكسا ماس
الفصل 26
بولنت جورينك
الفصل 27
Gerard Marty Agwasca، Bruno Garcia del Blanco، Jaume Sagrista Sauleda
الفصل 28
آرثر أتشابيان ، كريستيان لابلاس ، كريم تازارورت
الفصل 29
كلوديو رونكو وزكريا ريتشي
الفصل 30
الدورة الدموية
سوزان برايس ، باسكال فرانكس
الفصل 31
أندرو مورلي سميث ، أندريه ر.
جون آر بيبر
الفصل 32
مايكل بي قيصر ، جريت فان دن بيرغي
الفصل 33
ريك جوسلينك ، جان روسيلر
الفصل 34
Arne P. Neirink، Patrick Ferdinand، Dirk Van Raemdonk، Mark Van de Velde
الجزء الخامس التشخيصات المخبرية في أمراض القلب ووحدات العناية المركزة الأخرى
الفصل 35
آلان س جاف
الفصل 36
Evangelos Giannitsis ، Hugo A. Catus
الفصل 37
راجيف تشودري ، كيفن شاه ، آلان ميزل
الفصل 38
آنا مات هواس ، إريك إل جروف ، ستين دالبي كريستنسن
الفصل 39
ماريو بلباني ومونيكا ماريا مين ،
مارتينا زانينوتو
الجزء 6 متلازمة الشريان التاجي الحادة
الفصل 40
لينا باديمون ، جيما فيلاجور
الفصل 41
كريستيان ثيجيسين ، جوزيف س. ألبرت ،
ألان س جاف ، هارفي د. وايت
الفصل 42
كيرت هوبر ، توم كوين
الفصل 43
أدريان تشيونغ ، غابرييل ستيج ، ستيفان ك.جيمس
الفصل 44
بيتر سناوي وفرانس فان دي ورف
الفصل 45
خوسيه لوبيز سيندون ، إستيبان لوبيز دي سا
الفصل 46
هيكتور بوينو ، خوسيه أ.بارابيس
الفصل 47
فيكتور كوتشكا وستين دالبي كريستنسن
وليام فاينز ، بيوتر تويشيك ، بيوتر فيديمسكي
الفصل 48
بيروز إم ديفيروالا ، فريدريش دبليو موهر
الفصل 49
هولجر ثييل ، أوي سيمر
الفصل 50
إيفا سوان ، يواكيم ألفريدسون ، صوفيا سيدرهولم لوسون
الجزء 7 قصور القلب الحاد
الفصل 51. قصور القلب الحاد: علم الأوبئة ، التصنيف والفيزيولوجيا المرضية
ديميتروس فارماكيس ، جون باريسيس ، جيراسيموس فيليباتوس
الفصل 52
جوناثان ر. دالزيل ، كوليت إي جاكسون ، جون جيه دبليو ماكموري ، روي جاردنر
الفصل 53
باسكال فرانكس ، ويلفريد مولينز ، جوهان ويغن
الفصل 54
أيكاتيريني إن فيزولي ، أنتونيس أ. بيتسيس
الجزء 8 عدم انتظام ضربات القلب
الفصل 55
كارلو لافال ، ريناتو بيترو ريتشي ، ماسيمو سانتيني
الفصل 56. الرجفان الأذيني وعدم انتظام ضربات القلب فوق البطيني
ديموسثينيس كاتريتسيس ، أ. جون جوم
الفصل 57
يواكيم ر.إرليش ، ستيفان إتش هونلوسر
الجزء 9 أمراض القلب والأوعية الدموية الحادة الأخرى
الفصل 58
ميشيل نوتسياس ، برنارد مايش
الفصل 59
جريجوري دوكروك ، فرانك تاني ، برنارد جونج ، أليك فاخانيان
الفصل 60
سوزان برايس ، بريان إف كيو ، لورنا سوان
الفصل 61
بارلا أستارتشي ، لوران دي كيركوف ، جبرين الخوري
الفصل 62
ديميتريوس ديميتريادس ، ليزلي كوباياشي ، ليديا لام
الفصل 63
باتريشيا بريسبتيرو ، دينيس زافالوني ، بينيديتا أغنولي
الجزء 10 الحالات الحادة المصاحبة
الفصل 64
لوتشيانو جاتينوني ، إليونورا كارلسو
الفصل 65
نازارينو جاليير ، الكسندرا ماينز ، ماسيميليانو بالازيني
الفصل 66
آدم توربيكي ، مارتن كورزينا ، ستافروس كونستانتينيدس
الفصل 67
ديدييه ليس ، شارلوت كوردونيير ، فاليريا كاسو
الفصل 68
صوفي أ.جيفرت ، إريك هوست ، جون إيه كيلوم
الفصل 69
إيف ديبافييه وديثير ميسوتين وجريت فان دن بيرغي
الفصل 70
بيير مانوتشيو مانوتشي
الفصل 71
جان بيير باساند ، فرانسوا شييل ، نيكولا مينيفو
الفصل 72
جوليان أرياس أورتيز ، رافائيل فافوري ، جان لويس فينسينت
الفصل 73
سيان جاغار وهيلين ليكوك
الفصل 74
جينيفر جوزيفي ، جون ماكفيرسون ، تشاد واجنر ، إي. ويسلي إيلي
الفصل 75
آناصوفيا موريت ، رافائيل فافوري ، آلان دوروشر
الفصل 76
مارتن باليك
الفصل 77. الإدارة المحيطة بالجراحة لمرضى الجراحة عالية الخطورة: جراحة القلب
ماركو رانوتشي ، سيرينيلا كاستلفيتشيو ، أندريا بالوتا
الفصل 78
جين وود ، مورين كاروثرز
دليل الموضوع
يشار إلى مؤشرات إجراء طرق البحث وفقًا للفئات: الفئة الأولى - الدراسات مفيدة وفعالة ؛ IIA - البيانات المتعلقة بالفائدة غير متسقة ، ولكن هناك المزيد من الأدلة لصالح فعالية الدراسة ؛ IIB - البيانات المتعلقة بالفائدة غير متسقة ، لكن فوائد الدراسة أقل وضوحًا ؛ ثالثا - البحث عديم الفائدة.
تتميز درجة الأدلة بثلاثة مستويات: المستوى أ - هناك العديد من التجارب السريرية العشوائية أو التحليلات التلوية ؛ المستوى ب - البيانات التي تم الحصول عليها في تجربة معشاة واحدة أو في تجارب غير معشاة ؛ المستوى ج - تستند التوصيات إلى اتفاق الخبراء.
- مع الذبحة الصدرية المستقرة أو غيرها من الأعراض المرتبطة بمرض الشريان التاجي ، مثل ضيق التنفس ؛
- مع مرض الشريان التاجي المستقر ، حاليًا بدون أعراض بسبب العلاج ؛
- المرضى الذين لوحظت عليهم الأعراض لأول مرة ، ولكن ثبت أن المريض يعاني من مرض مستقر مزمن (على سبيل المثال ، من سوابق المريض تبين أن هذه الأعراض كانت موجودة منذ عدة أشهر).
وبالتالي ، فإن مرض الشريان التاجي المستقر يشمل مراحل مختلفة من المرض ، باستثناء الحالة التي يتم فيها تحديد المظاهر السريرية عن طريق تجلط الشريان التاجي (متلازمة الشريان التاجي الحادة).
في حالة أمراض القلب التاجية المستقرة ، ترتبط أعراض الإجهاد أو التمارين مع تضيق الشريان التاجي الرئيسي الأيسر بنسبة تزيد عن 50٪ أو تضيق بنسبة تزيد عن 70٪ في واحد أو أكثر من الشرايين الرئيسية. تناقش هذه الطبعة من المبادئ التوجيهية الخوارزميات التشخيصية والإنذارية ليس فقط لمثل هذه التضيق ، ولكن أيضًا لضعف الأوعية الدموية الدقيقة وتشنج الشريان التاجي.
التعاريف والفيزيولوجيا المرضية
يتميز CAD المستقر بعدم التوافق بين الطلب على الأكسجين وتسليمه ، مما يؤدي إلى نقص تروية عضلة القلب ، والذي يحدث عادةً بسبب الإجهاد البدني أو العاطفي ، ولكنه يحدث أحيانًا بشكل عفوي.
ترتبط نوبات إقفار عضلة القلب بعدم الراحة في الصدر (الذبحة الصدرية). يشمل مرض الشريان التاجي المستقر أيضًا مرحلة غير مصحوبة بأعراض من مسار المرض ، والتي قد تنقطع بسبب تطور متلازمة الشريان التاجي الحادة.
ترتبط المظاهر السريرية المختلفة لـ CAD المستقر بآليات مختلفة ، بما في ذلك:
- انسداد الشرايين النخابية ،
- تشنج موضعي أو منتشر في الشريان بدون تضيق مستقر أو في وجود لوحة تصلب الشرايين ،
- ضعف الأوعية الدموية الدقيقة ،
- ضعف البطين الأيسر المرتبط باحتشاء سابق لعضلة القلب أو مع اعتلال عضلة القلب الإقفاري (سبات عضلة القلب).
يمكن دمج هذه الآليات في مريض واحد.
الدورة الطبيعية والتوقعات
في مجموعة من المرضى الذين يعانون من مرض الشريان التاجي المستقر ، قد يختلف التشخيص الفردي اعتمادًا على الخصائص السريرية والوظيفية والتشريحية.
من الضروري تحديد المرضى الذين يعانون من أشكال أكثر شدة من المرض ، والذين قد يكون تشخيصهم أفضل مع التدخل العدواني ، بما في ذلك إعادة تكوين الأوعية الدموية. من ناحية أخرى ، من المهم تحديد المرضى الذين يعانون من أشكال خفيفة من المرض والتشخيص الجيد ، حيث يجب تجنب التدخلات الغازية غير الضرورية وإعادة التوعي.
تشخبص
يشمل التشخيص التقييم السريري ودراسات التصوير وتصوير الشرايين التاجية. يمكن استخدام الدراسات لتأكيد التشخيص في المرضى الذين يشتبه في إصابتهم بمرض الشريان التاجي ، وتحديد أو استبعاد الحالات المرضية المشتركة ، وتصنيف المخاطر ، وتقييم فعالية العلاج.
أعراض
عند تقييم ألم الصدر ، يتم استخدام تصنيف Diamond A.G. (1983) ، والتي بموجبها يتم تمييز الذبحة الصدرية غير النمطية والألم غير القلبي. يكشف الفحص الموضوعي للمريض المصاب بالذبحة الصدرية المشتبه بها فقر الدم ، وارتفاع ضغط الدم الشرياني ، وآفات الصمامات ، واعتلال عضلة القلب الضخامي الانسدادي ، واضطرابات النظم.
من الضروري تقييم مؤشر كتلة الجسم ، وتحديد أمراض الأوعية الدموية (النبض في الشرايين المحيطية ، والضوضاء في الشرايين السباتية والفخذ) ، وتحديد الحالات المرضية المصاحبة مثل أمراض الغدة الدرقية وأمراض الكلى ومرض السكري.
طرق البحث غير الغازية
يعتمد الاستخدام الأمثل للاختبار غير الجراحي على تقييم احتمالية الاختبار المسبق لـ CAD. بمجرد تحديد التشخيص ، تعتمد الإدارة على شدة الأعراض والمخاطر وتفضيل المريض. من الضروري الاختيار بين العلاج الدوائي وإعادة تكوين الأوعية ، واختيار طريقة إعادة تكوين الأوعية الدموية.
تشمل الدراسات الرئيسية للمرضى الذين يشتبه في إصابتهم بأمراض القلب التاجية الاختبارات الكيميائية الحيوية القياسية ، وتخطيط القلب ، ومراقبة تخطيط القلب على مدار 24 ساعة (إذا اشتبه في أن الأعراض مرتبطة باضطراب النظم الانتيابي) ، وتخطيط صدى القلب ، وفي بعض المرضى ، تصوير الصدر بالأشعة السينية. يمكن إجراء هذه الاختبارات في العيادة الخارجية.
تخطيط صدى القلبيوفر معلومات حول بنية ووظيفة القلب. في حالة وجود الذبحة الصدرية ، من الضروري استبعاد تضيق الأبهر وتحت الأبهر. الانقباض العالمي هو عامل تنبؤي في مرضى CAD. يعد تخطيط صدى القلب مهمًا بشكل خاص في المرضى الذين يعانون من النفخات القلبية واحتشاء عضلة القلب وأعراض قصور القلب.
وبالتالي ، يُستطب تخطيط صدى القلب عبر الصدر لجميع المرضى من أجل:
- استبعاد سبب بديل للذبحة الصدرية ؛
- الكشف عن انتهاكات الانقباض المحلي ؛
- قياسات الكسر الطرد (EF) ؛
- تقييم وظيفة البطين الأيسر الانبساطي (الفئة الأولى ، مستوى الدليل ب).
لا يوجد ما يشير إلى تكرار الدراسات في المرضى الذين يعانون من مرض الشريان التاجي غير المصحوب بمضاعفات في حالة عدم وجود تغييرات في الحالة السريرية.
الفحص بالموجات فوق الصوتية للشرايين السباتيةضروري لتحديد سمك المركب الداخلي للوسائط و / أو لوحة تصلب الشرايين في المرضى الذين يشتبه في إصابتهم بمرض الشريان التاجي (الفئة IIA ، مستوى الدليل C). يعد اكتشاف التغييرات مؤشرًا على العلاج الوقائي ويزيد من احتمال الاختبار المسبق لـ CAD.
المراقبة اليومية لتخطيط القلبنادرا ما يقدم معلومات إضافية مقارنة مع ممارسة اختبارات تخطيط القلب. الدراسة ذات قيمة في المرضى الذين يعانون من الذبحة الصدرية المستقرة وعدم انتظام ضربات القلب المشتبه به (الفئة الأولى ، مستوى الدليل C) وفي الذبحة الصدرية التشنجية الوعائية المشتبه بها (الفئة IIA ، مستوى الدليل C).
الفحص بالأشعة السينيةيشار إليه في المرضى الذين يعانون من أعراض غير نمطية ومرض رئوي مشتبه به (الفئة الأولى ، مستوى الدليل C) وفي قصور القلب المشتبه به (الفئة IIA ، مستوى الدليل C).
نهج خطوة بخطوة لتشخيص CAD
الخطوة الثانية هي استخدام طرق غير جراحية لتشخيص مرض الشريان التاجي أو تصلب الشرايين غير الانسدادي في المرضى الذين لديهم احتمالية متوسطة للإصابة بمرض الشريان التاجي. عندما يتم تحديد التشخيص ، يلزم العلاج الدوائي الأمثل وتصنيف المخاطر لأحداث القلب والأوعية الدموية.
الخطوة 3 - اختبارات غير جراحية لتحديد المرضى الذين يكون التدخل الجراحي وإعادة التوعي أكثر فائدة. اعتمادًا على شدة الأعراض ، يمكن إجراء تصوير الأوعية التاجية المبكر (CAG) مع تجاوز الخطوتين 2 و 3.
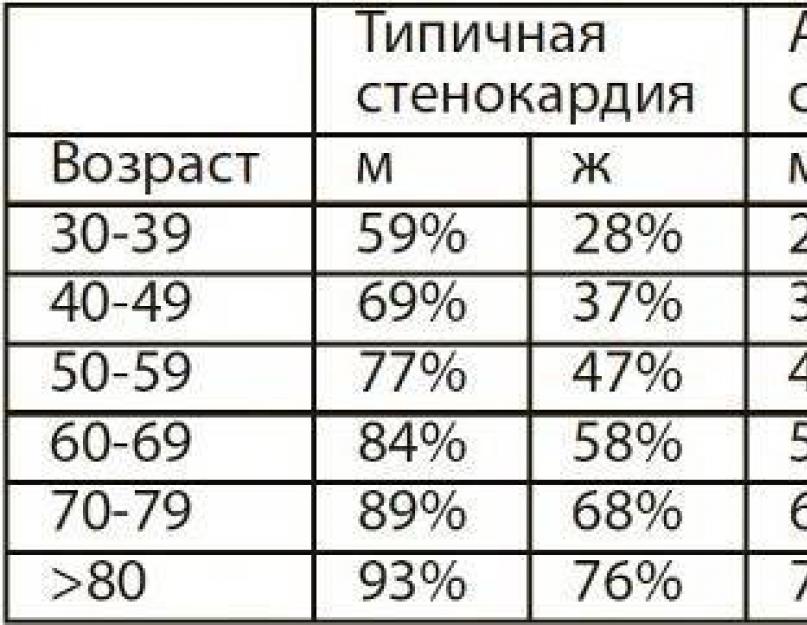
يتم تقدير احتمال الاختبار القبلي مع الأخذ في الاعتبار العمر والجنس والأعراض (الجدول).

مبادئ استخدام الاختبارات غير الغازية
تبلغ حساسية ونوعية اختبارات التصوير غير الجراحي 85٪ ، وبالتالي فإن 15٪ من النتائج كانت إيجابية كاذبة أو سلبية كاذبة. في هذا الصدد ، لا يوصى باختبار المرضى الذين يعانون من انخفاض (أقل من 15٪) وعالي (أكثر من 85٪) احتمالية اختبار الشريان التاجي.
اختبارات مخطط كهربية القلب أثناء التمرين لها حساسية منخفضة (50٪) وخصوصية عالية (85-90٪) ، لذلك لا ينصح بإجراء الاختبارات للتشخيص في المجموعة ذات الاحتمالية العالية لـ CAD. في هذه المجموعة من المرضى ، يكون الهدف من إجراء اختبارات تخطيط القلب للضغط هو تقييم الإنذار (التقسيم الطبقي للمخاطر).
يتم علاج المرضى الذين يعانون من انخفاض EF (أقل من 50 ٪) والذبحة الصدرية النموذجية باستخدام CAG بدون اختبارات غير جراحية ، لأنهم معرضون بشدة لخطر الإصابة بأمراض القلب والأوعية الدموية.
يجب على المرضى الذين لديهم احتمالية منخفضة جدًا للإصابة بأمراض القلب التاجية (أقل من 15٪) استبعاد الأسباب الأخرى للألم. مع وجود احتمال متوسط (15-85٪) ، يشار إلى الاختبارات غير الغازية. في المرضى الذين لديهم احتمالية عالية (أكثر من 85 ٪) ، يكون الاختبار ضروريًا لتقسيم المخاطر إلى طبقات ، ولكن في الذبحة الصدرية الشديدة ، يُنصح بإجراء CAG بدون اختبارات غير جراحية.
إن القيمة التنبؤية السلبية العالية جدًا للتصوير المقطعي (CT) تجعله مهمًا للمرضى الذين يعانون من انخفاض متوسط المخاطر (15-50٪).
الإجهاد ECG
يظهر VEM أو جهاز المشي عند احتمال الاختبار المسبق بنسبة 15-65٪. يتم إجراء الاختبار التشخيصي عند التوقف عن تناول الأدوية المضادة للإقفار. حساسية الاختبار 45-50٪ ، النوعية 85-90٪.
لم تتم الإشارة إلى الدراسة في حالة الحصار المفروض على كتلة فرع الحزمة اليسرى ، متلازمة WPW ، وجود جهاز تنظيم ضربات القلب بسبب عدم القدرة على تفسير التغييرات في المقطع ST.
لوحظت نتائج إيجابية كاذبة مع تغيرات تخطيط القلب المرتبطة بتضخم البطين الأيسر ، واضطرابات الكهارل ، واضطرابات التوصيل داخل البطيني ، والرجفان الأذيني ، والديجيتال. عند النساء ، تكون حساسية وخصوصية الاختبارات أقل.
في بعض المرضى ، يكون الاختبار غير مفيد بسبب الفشل في تحقيق معدل ضربات القلب دون الحد الأقصى في غياب أعراض نقص التروية ، مع وجود قيود مرتبطة بجراحة العظام ومشاكل أخرى. بديل لهؤلاء المرضى هو طرق التصوير ذات العبء الدوائي.
- لتشخيص مرض الشريان التاجي لدى مرضى الذبحة الصدرية ومتوسط احتمال الإصابة بمرض الشريان التاجي (15-65٪) الذين لا يتلقون الأدوية المضادة لنقص التروية ، والذين يمكنهم ممارسة الرياضة وليس لديهم تغييرات في مخطط كهربية القلب لا تسمح بتفسير التغيرات الدماغية (الفئة الأولى ، مستوى الدليل ب) ؛
- لتقييم فعالية العلاج في المرضى الذين يتلقون العلاج المضاد لنقص التروية (الفئة IIA ، المستوى C).
تخطيط صدى القلب بالإجهاد والتصوير الومضاني لتروية عضلة القلب
يتم إجراء تخطيط صدى القلب عند الإجهاد باستخدام النشاط البدني (VEM أو جهاز المشي) أو المستحضرات الدوائية. التمرينات فسيولوجية أكثر ، لكن التمارين الدوائية مفضلة عند ضعف الانقباض أثناء الراحة (الدوبوتامين لتقييم عضلة القلب القابلة للحياة) أو في المرضى غير القادرين على ممارسة الرياضة.
مؤشرات لتخطيط صدى القلب الإجهاد:
- لتشخيص مرض الشريان التاجي في المرضى الذين لديهم احتمال اختبار مسبق بنسبة 66-85٪ أو مع EF<50% у больных без стенокардии (Класс I, уровень доказанности В);
- لتشخيص نقص التروية في المرضى الذين يعانون من تغيرات في مخطط كهربية القلب أثناء الراحة والتي لا تسمح بتفسير مخطط كهربية القلب أثناء اختبارات التمرين (الفئة الأولى ، مستوى الدليل ب) ؛
- يُفضل اختبار الإجهاد باستخدام تخطيط صدى القلب على الاختبار الدوائي (الفئة الأولى ، مستوى الدليل C) ؛
- في المرضى الذين يعانون من أعراض وخضعوا للتدخل عن طريق الجلد (PCI) أو تطعيم مجازة الشريان التاجي (CABG) (الفئة IIA ، مستوى الدليل B) ؛
- لتقييم الأهمية الوظيفية للتضيق المعتدل المكتشف في CAH (الفئة IIA ، مستوى الدليل B).
يكشف التصوير الومضاني للتروية (BREST) مع التكنيشيوم (99mTc) عن نقص انسياب عضلة القلب أثناء التمرين مقارنةً بالتروية أثناء الراحة. من الممكن إثارة نقص التروية عن طريق النشاط البدني أو الدواء باستخدام الدوبوتامين والأدينوزين.
ترتبط الدراسات التي أجريت على الثاليوم (201T1) بحمل إشعاعي أعلى وتستخدم حاليًا بشكل أقل. مؤشرات التصوير الومضاني للتروية مماثلة لتلك المستخدمة في تخطيط صدى القلب بالإجهاد.
يتميز التصوير المقطعي بالإصدار البوزيتروني (PET) بمزايا تتفوق عليه من حيث جودة الصورة ، ولكنه يصعب الوصول إليه.
تقنيات غير جراحية لتقييم تشريح الشريان التاجي
يمكن إجراء التصوير المقطعي المحوسب بدون حقن التباين (يتم تحديد ترسب الكالسيوم في الشرايين التاجية) أو بعد الحقن الوريدي لعامل تباين يحتوي على اليود.
ترسب الكالسيوم هو نتيجة لتصلب الشرايين التاجية ، إلا في المرضى الذين يعانون من القصور الكلوي. عند تحديد الكالسيوم التاجي ، يتم استخدام مؤشر Agatston. ترتبط كمية الكالسيوم مع شدة تصلب الشرايين ، لكن الارتباط بدرجة التضيق ضعيف.
يسمح لك تصوير الأوعية التاجية بالتصوير المقطعي المحوسب باستخدام عامل تباين بتقييم تجويف الأوعية. الشروط هي قدرة المريض على حبس أنفاسه ، وغياب السمنة ، وإيقاع الجيوب الأنفية ، وسرعة ضربات القلب أقل من 65 في الدقيقة ، وغياب التكلس الشديد (مؤشر أجاتستون)< 400).
النوعية تقل مع زيادة الكالسيوم التاجي. يعد إجراء تصوير الأوعية المقطعية المحوسبة غير عملي عندما يكون مؤشر أجاتستون> 400. القيمة التشخيصية للطريقة متاحة في المرضى الذين يعانون من الحد الأدنى من متوسط احتمالية الإصابة بأمراض الشريان التاجي.
تصوير الأوعية التاجية
نادرًا ما تكون هناك حاجة إلى CAG للتشخيص في المرضى المستقرين. يشار إلى الدراسة إذا كان المريض لا يمكن أن يخضع لأساليب بحث التصوير بالضغط ، مع EF أقل من 50 ٪ والذبحة الصدرية النموذجية ، أو في الأشخاص ذوي المهن الخاصة.
يشار إلى CAG بعد التقسيم الطبقي للمخاطر غير الغازية في المجموعة عالية المخاطر لتحديد مؤشرات إعادة تكوين الأوعية الدموية. في المرضى الذين لديهم احتمالية عالية قبل الاختبار وذبحة صدرية شديدة ، يشار إلى تصوير الأوعية التاجية المبكر بدون اختبارات سابقة غير جراحية.
لا ينبغي إجراء CAG في المرضى الذين يعانون من الذبحة الصدرية الذين يرفضون PCI أو CABG أو الذين لن يؤدي إعادة تكوين الأوعية الدموية إلى تحسين الحالة الوظيفية أو نوعية الحياة.
الذبحة الصدرية الدقيقة
يجب الاشتباه في الذبحة الصدرية الأولية الدقيقة في المرضى الذين يعانون من الذبحة الصدرية النموذجية ، واختبارات تخطيط القلب الإيجابي أثناء ممارسة الرياضة ، وعدم تضيق الشريان التاجي النخابي.
البحث المطلوب لتشخيص الذبحة الصدرية الدقيقة:
- تخطيط صدى القلب الإجهاد مع التمرين أو الدوبوتامين لاكتشاف اضطرابات الانقباض الموضعية أثناء نوبة الذبحة الصدرية وتغييرات المقطع ST (الفئة IIA ، مستوى الدليل C) ؛
- تخطيط صدى القلب الدوبلري عبر الصدر للشريان النازل الأمامي مع قياس تدفق الدم التاجي الانبساطي بعد إعطاء الأدينوزين في الوريد وفي حالة الراحة للتقييم غير الجراحي لاحتياطي الشريان التاجي (الفئة IIB ، مستوى الدليل C) ؛
- CAG مع إعطاء الأسيتيل كولين والأدينوزين داخل التاج في الشرايين التاجية الطبيعية لتقييم احتياطي الشريان التاجي وتحديد الأوعية الدموية الدقيقة والتشنج النخابي (الفئة IIB ، مستوى الدليل C).
الذبحة الصدرية Vasospastic
للتشخيص ، من الضروري تسجيل مخطط كهربية القلب أثناء نوبة الذبحة الصدرية. يشار CAG لتقييم الشرايين التاجية (الفئة الأولى ، مستوى الدليل C). مراقبة تخطيط القلب على مدار 24 ساعة للكشف عن ارتفاع مقطع ST في حالة عدم وجود زيادة في معدل ضربات القلب (الفئة IIA ، مستوى الدليل C) و CAG مع إعطاء الأسيتيل كولين أو الإرغونوفين داخل التاج لتحديد تشنج الشريان التاجي (الفئة IIA ، مستوى الدليل C) .
في 3-4 يونيو 2005 ، في بوتشا ، مؤتمر علمي وعملي لمجموعة العمل المعنية بأمراض القلب الطارئة التابعة لجمعية أطباء القلب في أوكرانيا ، المدرجة في سجل الأحداث العلمية والعملية لوزارة الصحة الأوكرانية لعام 2005 ، تم عقده. استعرض المؤتمر الآليات الفيزيولوجية المرضية الرئيسية لمتلازمات الشريان التاجي الحادة (ACS) ، وفشل القلب الحاد (HF) ، وعدم انتظام ضربات القلب البطيني الذي يهدد الحياة والموت القلبي المفاجئ ، بالإضافة إلى تحليل أحدث الأبحاث في هذا المجال فيما يتعلق بتشخيص وعلاج والوقاية من أمراض القلب. أمراض القلب والأوعية الدموية (CVD).).
من إعداد إيرينا ستارنكايا
المهام الرئيسية لمجموعة العمل هي تطوير وتنفيذ الدلائل الإرشادية الوطنية لعلاج ACS و HF الحاد ، وتحديد الأساليب الحديثة العقلانية للتقسيم الطبقي وعلاج الأمراض القلبية الوعائية الأخرى ، ومراجعة إمكانيات الرعاية الطارئة في أمراض القلب . ركز المشاركون في المؤتمر بشكل أساسي على القواعد والمعايير الدولية للعلاج والتشخيص ، وبالتالي ، في التقارير والمناقشات ، تم إيلاء الاهتمام الرئيسي لتحليل ومناقشة توصيات الخبراء الأوروبيين والأمريكيين ، وبالتالي إمكانية تطبيقها. في أوكرانيا.
تم تقديم منحة تعليمية للمؤتمر من قبل Sanofi-Aventis و Boehringer-Ingelheim و Orion. نقدم استعراضًا موجزًا للخطب الأكثر إثارة للاهتمام لاهتمام قرائنا.
عضو مجلس إدارة الجمعية الأوروبية لأمراض القلب ، ورئيس الفريق العامل المعني بأمراض القلب في حالات الطوارئ التابع لجمعية أطباء القلب في أوكرانيا ، ورئيس قسم الإنعاش والعناية المركزة في معهد أمراض القلب الذي يحمل اسم A.I. اختصار الثاني. Strazhesko من أكاديمية العلوم الطبية في أوكرانيا ، دكتوراه في العلوم الطبية ، البروفيسور أولكسندر نيكولايفيتش باركهومينكو.
- تجري حاليًا مناقشة مسودة المبادئ التوجيهية الوطنية للعلاج والتشخيص ، بناءً على توصيات الجمعية الأوروبية لأمراض القلب (ESC) ، من قبل أعضاء مجموعة العمل ويتم إعدادها للنشر. من أجل التعامل مع مثل هذه الوثيقة المهمة بمسؤولية كاملة ، من الضروري دراسة توصيات المجلس الاقتصادي والاجتماعي بعناية ، وتسليط الضوء على الجوانب الأكثر صلة بأوكرانيا ، وتحديد المهام التي يمكن تحقيقها بشكل واقعي في ظروفنا.
تمت الموافقة على الدلائل الإرشادية الأوروبية لعلاج وتشخيص التهاب الكبد الوبائي الحاد مؤخرًا في أبريل من هذا العام. وفقًا لهذه الوثيقة ، يعتبر HF الحاد حالة مرتبطة بالتطور السريع لأعراض ومظاهر HF وينتج عن ضعف وظائف القلب على حد سواء دون علم الأمراض السابق وعلى خلفية أمراض القلب (الخلل القلبي المرتبط بكل من الانقباضي والانبساطي الاضطرابات ، عدم انتظام ضربات القلب ، التغيرات في ما قبل الحمل وبعده وأسباب أخرى). تتطلب هذه الحالة المهددة للحياة علاجًا عاجلاً. ومع ذلك ، فإن هذا التعريف ليس هو الأفضل. أدت محاولة الجمع بين جميع الجوانب الممكنة من HF الحاد إلى بعض الغموض والمصطلحات المبهمة. تميز إرشادات ESC هذه الأشكال من HF الحاد.
- HF الحاد اللا تعويضي (جديد أو مطور في أشكال مزمنة من HF) يتقدم ببطء ، خفيف نسبيًا ، بدون علامات صدمة قلبية ، وذمة رئوية ، أو أزمة ارتفاع ضغط الدم.
- يتجلى ارتفاع ضغط الدم الحاد HF في أعراض ضعف القلب على خلفية ارتفاع ضغط الدم ، ولكن كقاعدة عامة ، مع الحفاظ على وظيفة القلب الانقباضية وبدون وذمة رئوية.
- شكل مهم من HF الحاد هو الوذمة الرئوية ، تشخيصها يتطلب التحقق من التصوير الشعاعي. الوذمة الرئوية مصحوبة بمتلازمة الضائقة الشديدة ، خشخشة في الرئتين ، ضيق النفس ، تشبع الأكسجين أقل من 90٪ قبل العلاج.
- إن أشد أشكال HF الحاد هو الصدمة القلبية ، والتي تتجلى في انخفاض حاد في النتاج القلبي ، ونتيجة لذلك ، نقص تدفق الدم في الأنسجة. علامات الصدمة القلبية معروفة جيداً: انخفاض ضغط الدم إلى ما دون 90 ملم زئبق. الفن ، معدل ضربات القلب - أقل من 60 نبضة / دقيقة ، إدرار البول - أقل من 0.5 مل / كجم / ساعة.
- عادة ما ترتبط متلازمة النتاج القلبي المرتفع بتسرع القلب بشكل كبير (مع عدم انتظام ضربات القلب ، والتسمم الدرقي ، وفقر الدم ، ومتلازمة باجيت ، والتدخلات العلاجية المنشأ). من سمات هذا النوع من قصور القلب الحاد الأنسجة المحيطية "الدافئة" ، وارتفاع معدل ضربات القلب ، وأحيانًا انخفاض ضغط الدم.
- تتجلى متلازمة فشل البطين الأيمن في انخفاض النتاج القلبي ، وارتفاع الضغط في الوريد الوداجي ، وتضخم الكبد ، وانخفاض ضغط الدم الشرياني.
في أوروبا ، يتم إدخال 40٪ من المرضى الذين يتلقون العلاج في المستشفى بسبب ارتفاع ضغط الدم الحاد إلى المستشفى بسبب ضيق التنفس ، وهي الشكوى الرئيسية للمرضى. من بين مظاهر قصور القلب الحاد ، المرتبة الثانية هي تطور قصور القلب المزمن (تفاقم ضيق التنفس ، وذمة ، وضعف ، إلخ). وتجدر الإشارة إلى أن العديد من المرضى يدخلون المستشفى على خلفية قصور القلب المستقر ، مع نسبة طرد تزيد عن 40٪. لذلك ، في تشخيص HF الحاد ، من المستحيل التركيز فقط على الدراسات القياسية ، فمن الضروري البحث بنشاط عن سبب حالة المريض ، حتى في حالة عدم وجود علامات واضحة على ضعف القلب.
يعتمد تشخيص HF الحاد على الأعراض والفحص السريري للمريض ، ويتم لعب دور مهم بواسطة تخطيط القلب والأشعة السينية واختبارات الدم للعلامات البيولوجية وتخطيط صدى القلب الدوبلري. أصبحت طرق البحث المخبري ذات أهمية متزايدة في تشخيص أمراض القلب. لذلك ، في جميع المرضى الذين يعانون من HF الحاد ، يوصى بالتأكيد بإجراء تعداد دم كامل ، وتحديد عدد الصفائح الدموية ، وجلوكوز الدم ، واليوريا ، والكرياتينين ، والكهارل ، و CRP ، و D-dimer ، والتروبونين. يجري النظر في مسألة الإدخال الواسع لتحليل الببتيد الناتريوتريك في البلازما في HF الحاد ، والذي يتجلى بشكل رئيسي في ضيق التنفس. في حالة الخلل القلبي الشديد ، وكذلك مع مرض السكري المصاحب ، من المهم الانتباه إلى مؤشرات غازات الدم الشرياني ، في حالة خطيرة وعلى خلفية تناول مضادات التخثر - على INR (النسبة الزمنية الدولية للثرومبوبلاستين الطبيعي).
المبادئ الأساسية لعلاج HF الحاد هي كما يلي.
- توفير التهوية والأكسجين.
- العلاج الطبي:
- المورفين ونظائره مع ركود شديد في الدورة الدموية الرئوية.
- العلاج المضاد للتخثر للـ ACS والرجفان الأذيني.
- موسعات الأوعية لمكافحة نقص انسياب الأنسجة المحيطية (النترات ، نيتروبروسيد الصوديوم ، نسيريتيد - الببتيد المدون للصوديوم البشري المؤتلف ، مضادات الكالسيوم) ؛
- مثبطات إيس؛
- مدرات البول.
- β حاصرات.
- الأدوية المؤثرة في التقلص العضلي (الدوبامين ، الدوبوتامين ، مثبطات الفوسفوديستيراز ، الليفوسيميندان ، الإبينفرين ، النوربينفرين ، جليكوسيدات القلب).
- نادرا ما يشار إلى العلاج الجراحي (على سبيل المثال ، مع تمزق الحاجز بين البطينين بعد الاحتشاء ، قلس الصمام المترالي الحاد).
- استخدام الأجهزة المساعدة الميكانيكية (معاكسة النبضات بالبالون داخل الأبهر) أو زرع القلب.
المرضى الذين يعانون من HF الحاد قد يستجيبون جيدًا للعلاج ، اعتمادًا على سبب HF. لكن حتى في هذه الحالات ، يحتاجون إلى علاج طويل الأمد ومراقبة المتخصصين.
تم افتتاح الاجتماع المخصص لـ ACS من قبل رئيس قسم احتشاء عضلة القلب وعلاج إعادة التأهيل في معهد أمراض القلب الذي يحمل اسم A.I. اختصار الثاني. Strazhesko من أكاديمية العلوم الطبية في أوكرانيا ، دكتوراه في العلوم الطبية ، البروفيسور فالنتين ألكساندروفيتش شوماكوف ، الذي تحدث عن المشاكل والآفاق الحديثة لتشخيص وعلاج ACS دون ارتفاع مقطع ST.
- في 2 مليون مريض في الولايات المتحدة مع عيادة ACS ، تم الكشف عن علامات ECG لإصابة عضلة القلب الحادة: 600 ألف مع ارتفاع مقطع ST ؛ الباقي - بدونها. يزداد خطر الإصابة بالـ ACS مع تقدم العمر: كما هو موضح بواسطة S. Kulkarni et al. (ACC ، 2003 ، CRUSADE Presentation) ، في الأشخاص الذين تزيد أعمارهم عن 75 عامًا ، يزداد خطر الوفاة ، وتطور احتشاء عضلة القلب (MI) ، و HF بشكل كبير. من الأهمية بمكان وجود مرض السكري ، والذي يزيد أيضًا من خطر الإصابة بالـ ACS ، كما هو موضح في نفس الدراسة.
يشمل مصطلح "متلازمة الشريان التاجي الحادة":
- الذبحة الصدرية غير المستقرة وغير Q-MI ؛
- Q-IM ؛
- الموت القلبي المفاجئ؛
- المضاعفات الإقفارية الحادة للقسطرة والدعامات والتدخلات الأخرى على الشرايين التاجية.
في السنوات الأخيرة ، شهد فهم الآلية المرضية للـ ACS عددًا من التغييرات ، على وجه الخصوص ، تم إيلاء الكثير من الاهتمام لعوامل الالتهاب الجهازي والمحلي ، مما يساهم في زعزعة استقرار اللويحات الدهنية. يؤدي تكوينه وتمزقه وتآكله ، وتجلط الدم اللاحق ، وتضيق الأوعية إلى نقص التروية ، وتلف ، ونخر في خلايا القلب ، ونتيجة لذلك ، إلى خلل في عضلة القلب. يمكن أن تكون الأسباب المحتملة للالتهاب الجهازي التي تساهم في زعزعة استقرار اللويحة الدهنية هي الإجهاد التأكسدي (التشعيع ، والحمل النفسي والعاطفي والبدني ، وأخطاء النظام الغذائي) ، والإجهاد الديناميكي ، والتعرض للعوامل المعدية ، بما في ذلك تفاقم الأمراض الالتهابية المزمنة ، والجهاز المناعي و ردود الفعل التحسسية. يحدث تنشيط التهاب جدار الأوعية الدموية بواسطة LDL المؤكسد بمشاركة المقيمين المنشط (الصاري) وخلايا الدم الالتهابية المهاجرة ، مع إطلاق الإنزيمات المحللة للبروتين (البروتياز المعدني) ، الجذور الحرة ، موت الخلايا المبرمج ونخر العناصر الخلوية للبلاك. في المستقبل ، يتشكل ورم دموي داخل اللويحة ، وينمو حجمها بسرعة ، وتزداد درجة تضيق الوعاء الدموي وفقًا لذلك. في النهاية ، يتم تدمير مصفوفة النسيج الضام وغطاء البلاك مع تطور تجلط الدم الموضعي.
وفقًا للآراء الجديدة حول الفيزيولوجيا المرضية للـ ACS ، تم إيلاء المزيد من الاهتمام لعوامل الالتهاب الجهازي في تشخيص وعلاج هذه الحالة المرضية. لذلك ، في تشخيص ACS ، يعتبر البروتين التفاعلي C والفيبرينوجين حاليًا علامات تشخيصية مهمة في IHD ، نظرًا لأن قيمة هذه المؤشرات مرتبطة بالوفيات في IHD غير المستقر (Lindahl et al. ، 2000).
في عام 2002 ، اعتمد ESC خوارزمية لإدارة المرضى الذين يشتبه في إصابتهم بالـ ACS ، والتي بموجبها ، بعد الاشتباه السريري في ACS ، يجب إجراء الفحص البدني الروتيني ، ومراقبة تخطيط القلب ، واختبارات الدم. إذا كان المريض يعاني من ارتفاع مستمر في ST ، يتم الإشارة إلى تجلط الدم أو التدخلات داخل الأوعية الدموية. في حالة عدم استمرار ارتفاع ST ، يتم وصف الهيبارين (وزن جزيئي منخفض أو غير مجزأ) للمرضى ، والأسبرين ، وكلوبيدوجريل ، وحاصرات بيتا ، والنترات ، ويتم حل درجة الخطر لدى المريض. إذا كان المريض معرضًا لخطر كبير ، فيجب وصف حاصرات مستقبلات البروتين السكري وإجراء تصوير البطين التاجي. في المستقبل ، بناءً على المتطلبات السريرية وتصوير الأوعية ، يتم إجراء التدخل داخل الأوعية الدموية أو تطعيم مجازة الشريان التاجي (CABG) أو استمرار العلاج بالعقاقير. في المرضى ذوي الخطورة المنخفضة ، يتم إعادة تحديد مستوى التروبونين في الدم ، وفقط إذا كانت نتيجة هذا الاختبار سلبية مرتين ، يتم تحديد مسألة أساليب العلاج الإضافية ، وإلا يتم علاج المريض بنفس الطريقة تمامًا كمرضى في المجموعة عالية الخطورة.
وبالتالي ، فإن من أهم الخطوات التي تحدد أساليب علاج المريض تحديد درجة الخطر. يبدو أن تحليل مخطط كهربية القلب هو أسهل طريقة لتقييم المخاطر (المرضى الذين يعانون من الاكتئاب أو ارتفاع ST ، بالإضافة إلى ارتفاع ارتفاع ST ، هم الأكثر عرضة للخطر) ؛ تزداد درجة الخطر أيضًا اعتمادًا على تواتر النوبات الإقفارية. يعتبر التروبونين علامة فعالة لزيادة المخاطر في متلازمة المتلازمة التنفسية الحادة. تشمل المجموعة عالية الخطورة أيضًا المرضى الذين يعانون من الذبحة الصدرية غير المستقرة التي تلي الاحتشاء المبكر ، مع ديناميكيات الدم غير المستقرة خلال فترة المراقبة ، مع عدم انتظام ضربات القلب الحاد (نوبات متكررة من عدم انتظام دقات القلب البطيني ، والرجفان البطيني) ، وداء السكري ، وكذلك مع رسومات تخطيط القلب التي لا تصنع من الممكن تقييم التغييرات في مقطع ST. المرضى المعرضون لخطر منخفض هم أولئك الذين لا يعانون من نوبات متكررة من ألم الصدر أثناء المتابعة ، ولا يوجد اكتئاب أو ارتفاع ST ، ولكن انعكاس الموجة T ، أو موجات T المسطحة ، أو تخطيط القلب الطبيعي ، ولا يوجد ارتفاع تروبونين أو علامات كيميائية حيوية أخرى.
إدارة المرضى المعرضين لمخاطر عالية على النحو التالي. أثناء التحضير لتصوير الأوعية ، من الضروري إعطاء الهيبارين منخفض الوزن الجزيئي (enoxaparin) ، بالإضافة إلى حاصرات مستقبلات GP IIb / IIIa ، والتي يستمر تأثيرها 12 (absiximab) أو 24 (tirofiban ، eptifibatide) في الحالة من قسطرة. إذا تمت الإشارة إلى المريض من أجل RSI ، فمن المعقول وصف عقار كلوبيدوجريل ، ولكن إذا تم التخطيط لـ CABG ، فيجب إيقاف عقار كلوبيدوجريل قبل 5 أيام من العملية المقترحة.
لطالما تم تقدير مزايا الهيبارين منخفض الوزن الجزيئي (LMWH) من قبل الأطباء من جميع التخصصات. تتميز بإمكانية التنبؤ بشكل أفضل للتأثير المضاد للتخثر مقارنة بالهيبارين التقليدي بسبب نقص الارتباط ببروتينات البلازما وأغشية الخلايا البطانية. وفقًا لذلك ، لا يتطلب علاج LMWH مثل هذه المراقبة المخبرية الفردية الدقيقة. تتمتع LMWHs بتوافر حيوي مرتفع (يصل إلى 90٪ بعد الحقن العميق تحت الجلد) ، مما يسمح بإعطائها تحت الجلد ليس فقط للوقاية ولكن أيضًا للأغراض العلاجية ، بالإضافة إلى نشاط مضاد للتخثر أطول (عمر النصف أكثر من 4.5 ساعة بعد عن طريق الوريد مقابل 50-60 دقيقة للهيبارين التقليدي) مع تعيين 1-2 مرات في اليوم.
في دراسة ESSENCE (M. كانت الأحداث في مجموعة enoxaparin أقل بشكل ملحوظ بحلول اليوم 14 ، واستمرت الاختلافات بين المرضى في enoxaparin ومجموعات الدواء الوهمي بحلول اليوم 30. وفقًا لبعض التقارير ، فإن الكفاءة العالية لـ enoxaparin تستمر حتى بعد عام (Fox KAA. Heart ، 1998).
وبالتالي ، فإن Enoxaparin ، وفقًا لتجارب عشوائية متعددة المراكز ، خاضعة للتحكم الوهمي ، هو LMWH الوحيد الذي ثبت أنه أكثر فعالية من الهيبارين غير المجزأ.
أظهرت دراسة ARMADA ، وهي مقارنة عشوائية لتأثير enoxaparin و dalteparin والهيبارين غير المجزأ على علامات تنشيط الخلية في المرضى الذين يعانون من ACS دون ارتفاع مقطع ST ، أن enoxaparin فقط كان له تأثير إيجابي على ديناميكيات جميع العلامات الثلاثة. على الرغم من أن تصميم الدراسة لم يقارن معايير الفعالية السريرية ، إلا أن حدوث الوفاة ، وإعادة الاحتشاء ، ونقص التروية المتكرر كان أقل في مجموعة الإينوكسابارين (13٪) مقارنة بمجموعات الدالتارين (18.8٪) والهيبارين (27.7٪).
يجب التخطيط لتصوير الأوعية التاجية في أقرب وقت ممكن في حالة عدم وجود إلحاح لا داعي له. فقط في مجموعة صغيرة نسبيًا من المرضى ، يجب إجراء تصوير الأوعية التاجية في غضون الساعة الأولى: مع نقص التروية الحاد لفترات طويلة ، وعدم انتظام ضربات القلب الشديد ، وعدم استقرار الدورة الدموية. في حالات أخرى ، يتم تنفيذ هذه التقنية في غضون 48 ساعة أو أثناء الاستشفاء. في حالة وجود آفات ، يسمح تشريحها بإعادة توعية عضلة القلب ، بعد إجراء تقييم شامل لانتشار الضرر وخصائص أخرى للضرر ، يتم تحديد مسألة أساليب العلاج الإضافية.
تتكون إدارة المرضى ذوي المخاطر المنخفضة من الأدوية الفموية مثل الأسبرين ، كلوبيدوجريل (جرعة تحميل من كلوبيدوجريل 300 مجم ، ثم 75 مجم يوميًا) ، حاصرات بيتا ، وربما النترات ، ومضادات الكالسيوم. في هذه المجموعة من المرضى ، يوصى ببدء تدابير الوقاية الثانوية ، وإيقاف العلاج باستخدام LMWH ، إذا لم تكن هناك تغييرات في مخطط كهربية القلب في نهاية فترة المراقبة ، ولم يكشف التحليل الثاني المتتالي عن زيادة في نشاط التروبونين.
يجب أن تتضمن الإدارة طويلة المدى للمرضى الذين خضعوا للـ ACS عددًا من التدابير:
- تعديل قوي لعوامل الخطر ؛
- الأسبرين بجرعة 75-150 مجم. بالإضافة إلى ذلك ، مع الأخذ في الاعتبار نتائج دراسة كيور ، يتم تعيين عقار كلوبيدوجريل (بلافيكس) بجرعة 75 مجم لمدة 9 على الأقل ، أفضل من 12 شهرًا (في هذه الحالة ، يجب تقليل جرعة الأسبرين إلى 75-100 مجم) ؛
- تعمل حاصرات β على تحسين التشخيص في مرضى ما بعد MI ؛
- العلاج الخافض للدهون (مثبطات اختزال HMG-CoA تقلل بشكل كبير من معدل الوفيات واحتمال حدوث أحداث الشريان التاجي ، بينما لا يحدث فقط تراجع في عملية تصلب الشرايين ، ولكن أولاً وقبل كل شيء ، يتم تعطيل اللويحة الملتهبة ، وانحدار الخلل البطاني ، وانخفاض في نشاط العوامل التخثرية) ؛
- يمكن أن تلعب مثبطات الإنزيم المحول للأنجيوتنسين دورًا مستقلاً في الوقاية الثانوية من المتلازمات التاجية (SOLVD ، 1991 ؛ SAVE ، 1992 ؛ HOPE ، 2000) ، والتي قد يرتبط تأثيرها أيضًا بتثبيت اللويحة المتصلبة في الشرايين.
يستمر البحث عن طرق فعالة للعلاج والوقاية من أحداث الشريان التاجي. على وجه الخصوص ، تم الحصول على نتائج مثيرة للاهتمام من الدراسة حول تأثير التطعيم ضد الإنفلونزا في MI (FLUVACS). أظهرت الدراسة أثراً إيجابياً - تغير في الاستجابة المناعية لغزو فيروس الأنفلونزا فيما يتعلق بزعزعة استقرار مرض الشريان التاجي. تمت دراسة معدل الإصابة بأمراض القلب والأوعية الدموية أيضًا لدى الأشخاص المسجلين لدى ثلاث شركات تأمين في مينيابوليس - 140،055 في موسم 1998-1999. و 146.328 في موسم 1999-2000. في الوقت نفسه ، تم تطعيم حوالي نصف الأشخاص الذين تم فحصهم. أظهرت نتائج المقارنة انخفاضًا معنويًا في الوقوع (من حيث تواتر الاستشفاء) في الأفراد الملقحين (K.L. Nichol ، J. Nordin ، J. Mully et al. ، 2003). هناك أدلة على أن إضافة النبيذ الأحمر إلى العلاج التقليدي لمرضى ACS يزيد من قدرة مضادات الأكسدة في الدم ويحسن بشكل كبير وظيفة البطانة (E. Venegas ، F. Leighton ، الجامعة الكاثوليكية في تشيلي ، سانتياغو ، تشيلي).
تم تسليط الضوء على مشكلة ACS مع ارتفاع ST في تقريرها من قبل عضو مراسل في أكاديمية العلوم الطبية في أوكرانيا ، كبير أطباء القلب في وزارة الصحة في أوكرانيا ، رئيس قسم العلاج بالمستشفى رقم 1 في الجامعة الطبية الوطنية. أ. Bogomolets ، دكتوراه في العلوم الطبية ، الأستاذة إيكاترينا نيكولاييفنا أموسوفا.
- يرغب كل طبيب في أوكرانيا في علاج مرضاه وفقًا لأحدث التوصيات الأوروبية. في الوقت نفسه ، فإن التعرف على هذه التوصيات يسبب بعض الاستياء بين الأطباء المحليين ، لأنه من الصعب في ممارستنا اتباع المعايير الأوروبية للعلاج بسبب العديد من المشاكل المالية والتنظيمية. لذلك ، اليوم ، عندما يكون من المستحيل تحقيق المعايير المعتمدة في البلدان المتقدمة في العالم ، يجب على الأطباء الأوكرانيين أن يحددوا بأنفسهم الوسط الذهبي - حل وسط معقول بين متطلبات الخبراء الدوليين وواقع بلدنا.
بادئ ذي بدء ، يجب أن نكون على دراية بقيود العلاج الحالة للخثرة في مرضى ACS. يعتمد ضخه على مستوى الأنسجة بشكل كبير على عامل الوقت. لا تزال المشاكل الخطيرة في علاج التخثر هي تجلط الدم ، وإعادة الانسداد ، والتخثر المتبقي وتضيق الشريان التاجي ، والانصمام المجهري في السرير البعيد ، وظاهرة عدم الانسياب مع الشريان التاجي "المفتوح" ، ومضاعفات في شكل نزيف داخل الجمجمة.
حاليًا ، يتم تحديد فعالية العلاج حال التخثر سريريًا من خلال تقليل الألم أو اختفائه بشكل ملحوظ لدى المريض ، مع تحسن موضوعي في حالة المريض ، واتجاهات إيجابية على مخطط كهربية القلب. لا أحد تقريبًا يتعامل مع التحديد الدقيق لمدى اكتمال عملية إعادة ضخ الدم ، على الرغم من أن هذه مسألة مهمة للغاية في تقييم درجة خطورة المريض ، والتي تحدد توقيت خروج المريض من المستشفى ، والإحالة إلى تصوير الأوعية التاجية وغيرها. جوانب الرعاية. أود أن أؤكد أن المؤشر البسيط - ديناميكيات المقطع ST 60-180 دقيقة بعد فتح الشريان التاجي - هو معيار دقيق إلى حد ما لفعالية ضخه. تقييم ديناميات ST بسيط للغاية ، وبفضله يمكن للطبيب فهم مدى فعالية التدابير العلاجية لإعادة ضخ الدم.
ظهر مؤخرًا عامل حال تخثر جديد ، وهو tenecteplase ، في أوكرانيا. مزاياها واضحة: يتميز الدواء بخصوصية عالية من الفيبرين وزيادة عمر النصف في بلازما الدم ، مما يسمح بإعطاء tenecteplase كبلعة ، وبدء تحلل الخثرة حتى في مرحلة ما قبل دخول المستشفى. بالإضافة إلى ذلك ، فإن tenecteplase مقاوم لمثبطات منشط البلازمينوجين من النوع الأول. بالمقارنة مع الستربتوكيناز ، فإن إدخال tenecteplase يسمح في 80٪ من الحالات بتحقيق سالكية الشريان التاجي في كثير من الأحيان ، مما يضمن فعالية إكلينيكية أعلى. ولكن كيف تظهر هذه الفوائد في الواقع فيما يتعلق بالأداء السريري؟ كما هو موضح في العديد من الدراسات السريرية (GUSTO-I ، 1993 ؛ INJECT ، 1995 ؛ GUSTO-III ، 1997 ؛ ASSENT-2 ، 1999 ؛ في TIME-2 ، 2000) ، فإن الأدوية الحالة للتخثر لمجموعة منشطات البلازمينوجين النسيجية محدودة للغاية. زيادة الفعالية الإكلينيكية ، وجميع مزاياها بشكل أساسي في راحة الإعطاء وبعض التقليل من تكرار المضاعفات الشديدة للعلاج (النزيف داخل الجمجمة).
وهكذا ، حتى الآن ، فإن تحسين فعالية علاج إعادة التروية يتمثل في تحسين العلاج المساعد بمضادات الثرومبين ، والذي يهدف إلى منع تجلط الدم المبكر والمتأخر ، وتقليل وتيرة الانصمام المجهري للأوعية في السرير البعيد ، وزيادة اكتمال نضح الأنسجة. تشمل الأدوية المساعدة LMWH (enoxaparin) ومضادات التخثر غير المباشرة والأدوية المضادة للصفيحات.
حتى وقت قريب ، ركز العلاج المساعد على مجالين: استبدال الهيبارين غير المجزأ بـ LMWH واستخدام حاصرات مستقبلات بروتين سكري قوية للاندماج بأمان مع نصف جرعة مضادات التخثر. أدت هذه الإحالات الجديدة إلى عدد من الفوائد النهائية (إعادة الاحتشاء ، الوفيات) ، ولكن لسوء الحظ ، ارتبط استخدام عقار أبسيكسيماب بزيادة كبيرة في النزيف الرئيسي. لذلك ، لم يتم تضمين مثبطات مستقبلات البروتين السكري في التوصيات الأوروبية والأمريكية لعلاج التخثر.
يمكن تحقيق الحد من تكرار الانتكاسات بمساعدة أنظمة جديدة من العلاج الوقائي - أحد أكثر الأنظمة الواعدة هو النظام الذي يتضمن الإينوكسابارين. ومع ذلك ، حتى مع هذا المخطط ، لوحظ وجود تأثير سلبي - زيادة في وتيرة النزيف الخطير في مجموعة المرضى الذين تزيد أعمارهم عن 75 عامًا. بناءً على ذلك ، في التوصيات الأمريكية (2004) ، يكون استخدام الإينوكسابارين أكثر تقييدًا من تلك الأوروبية. لا ينصح الخبراء الأمريكيون بوصف الدواء للمرضى في هذه الفئة العمرية. مع أخذ ذلك في الاعتبار ، تم تعديل بروتوكول دراسة ExTRACT-TIMI-25 الكبيرة ، التي تشارك فيها أوكرانيا أيضًا - بالنسبة للمرضى الذين تزيد أعمارهم عن 75 عامًا ، تم استبعاد بلعة enoxaparin ، وتم تقليل جرعة الدواء إلى 0.75 مجم / كجم مرتين في اليوم (في حالات أخرى - 1 مجم / كجم). يجب أن تقدم هذه الدراسة إجابة نهائية لمسألة الفعالية النسبية لإينوكسابارين والهيبارين غير المجزأ في تحلل الخثرات. من المتوقع أن تكون نتائج الدراسة أساسية في الإصدار الجديد من التوصيات لاستخدام LMWH كعلاج مساعد لعلاج إعادة التروية.
يولي الخبراء الأوروبيون والأمريكيون اهتمامًا كبيرًا للعلاج المضاد للصفيحات. أكدت دراسة CLARITY-TIMI-28 ، التي انتهت هذا العام ، قيمة استخدام عقار كلوبيدوجريل بالإضافة إلى الأسبرين في ACS المرتفع ST ، والذي تم استخدامه سابقًا على نطاق واسع ، بدون قاعدة أدلة. أكدت الدراسة أن إضافة عقار كلوبيدوجريل إلى نظام العلاج يحسن سالكية الشريان التاجي أثناء ضخه ، ويقلل من تكرار حدوث احتشاء عضلة القلب ، على الرغم من أنه لم يكن من الممكن الحصول على فرق في الوفيات بسبب قلة عدد المرضى. علاوة على ذلك ، كان هذا التأثير هو نفسه ولم يعتمد على الجنس والعمر وتوطين الاحتشاء واستخدام مضادات التخثر والهيبارين. لوحظت الفوائد ليس فقط فيما يتعلق بإعادة التوعي ، ولكن أيضًا فيما يتعلق بإعادة ضخ الدم على مستوى الأنسجة ، وهو أكثر أهمية بكثير لبقاء المريض. مع مثل هذا العلاج القوي بمضادات الثرومبين ، تعد مؤشرات الأمان مهمة جدًا: كما اتضح ، لم يؤدي استخدام عقار كلوبيدوجريل إلى زيادة تواتر النزيف الحاد داخل الجمجمة ، على الرغم من زيادة تواتر النزيف غير الحاد بشكل طفيف.
تم إجراء دراسة مثيرة للاهتمام في الصين (COMMIT / CSS-2 ، 2005) ، والتي شملت حوالي 46000 مريض يعانون من احتشاء عضلي حاد يستمر لمدة تصل إلى 24 ساعة ، بغض النظر عما إذا كانوا قد تلقوا علاج التخثر أم لا (متوسط الوقت العشوائي كان 10 ساعات). نتيجة لذلك ، كشفت هذه الدراسة عن فروق ذات دلالة إحصائية في معدل الوفيات: مع استخدام عقار كلوبيدوجريل في نظام العلاج ، انخفض معدل الوفيات بشكل ملحوظ. النزيف الشديد في هذه الحالة كما في الدراسة السابقة لم يزيد من تواتره.
وبالتالي ، فإن تكثيف العلاج بمضادات الصفيحات من خلال استخدام عقار كلوبيدوجريل يفتح بعض الفرص الإضافية لأمراض القلب الطارئة في تحسين الفعالية السريرية لعلاج إعادة التروية. لذلك ، يعتزم أطباء القلب المحليون إثارة مسألة تضمين عقار كلوبيدوجريل في الدلائل الإرشادية الوطنية لعلاج احتشاء عضلة القلب. تعمل وزارة الصحة الأوكرانية حاليًا على تطوير برنامج وطني حول الأمراض القلبية الوعائية ، والذي من المقرر ، على وجه الخصوص ، أن يشمل العديد من الأدوية الحديثة وأنظمة العلاج. وبالتالي ، يمكن للمرضى الأوكرانيين أن يأملوا في الحصول على تمويل حكومي أكبر لأمراض القلب الطارئة أكثر من ذي قبل ، بما في ذلك إمكانية توفير أدوية عالية الفعالية مثل عقار كلوبيدوغريل. مما لا شك فيه أن تحسين النظام التنظيمي ، والذي سيسرع في بدء العلاج ، له أهمية كبيرة في تحسين الرعاية الطبية في أمراض القلب الطارئة.
تم تقديم عروض شيقة في الاجتماع المخصص لاضطراب نظم القلب في ممارسة طب القلب في حالات الطوارئ. وهكذا ، سمي رئيس قسم عدم انتظام ضربات القلب في معهد أمراض القلب باسمه. اختصار الثاني. Strazhesko من أكاديمية العلوم الطبية في أوكرانيا ، دكتور في العلوم الطبية ، البروفيسور Oleg Sergeevich Sychev في تقريره تطرق إلى مشكلة الإغماء (SS).
- نظرًا لتنوع الأسباب المحتملة لمرض التصلب العصبي المتعدد ، غالبًا ما يكون من الصعب تحديد المرض الأساسي. يقدم خبراء ESC برنامج فحص خاص لمثل هؤلاء المرضى. يعتمد التشخيص التفريقي إلى حد كبير على الاختلافات بين مسار الإغماء: سمات حالات ما قبل الإغماء وما بعده ، ومدة فقدان الوعي. غالبًا ما يحدث الإغماء العصبي بعد رؤية مفاجئة أو صوت أو رائحة كريهة ، في غضون ساعة واحدة بعد تناول الطعام ، مصحوبًا بالغثيان والقيء. يحدث الإغماء الوعائي المبهمي بسبب الإجهاد والألم الحاد والوقوف لفترات طويلة في وضع مستقيم (في حالة الانتباه أو في غرف خانقة). متلازمة الجيوب السباتية هي سبب شائع للإغماء عند الرجال الذين تزيد أعمارهم عن 60 عامًا ، والاختبار التشخيصي في هذه الحالة هو تدليك الجيوب السباتية. يمكن تسجيل الإغماء الانتصابي في وجود انخفاض ضغط الدم الانتصابي الموثق (انخفاض في ضغط الدم الانقباضي بمقدار 20 ملم زئبق أو عندما يكون ضغط الدم أقل من 90 ملم زئبق) بالاقتران مع حالة إغماء أو حالة ما قبل الإغماء. يمكن أن يكون إغماء نشأة عدم انتظام ضربات القلب من أصل مختلف - بسبب عدم انتظام دقات القلب ، وبطء القلب ، والحصار. لذلك ، من أجل التشخيص التفريقي للإغماء ، من الضروري إجراء تخطيط كهربية القلب: يتم تشخيص إغماء عدم انتظام ضربات القلب في وجود علامات بطء القلب (أقل من 40 نبضة / دقيقة) ، والحصار الجيبي الأذيني المتكرر مع توقف مؤقت لأكثر من 3 ثوانٍ ، والحصار الأذيني البطيني الثاني ( Mobitz II) أو الدرجة الثالثة ، تغييرات في حصار حزمة الساقين اليمنى واليسرى له ، عدم انتظام دقات القلب فوق البطيني الانتيابي ، عدم انتظام دقات القلب البطيني ، اضطرابات في عمل منظم ضربات القلب الاصطناعي مع وجود فترات توقف. يتم تحديد الإغماء الناتج عن علم الأمراض العضوية للقلب والأوعية الدموية من خلال تحديد المرض الأساسي ، والذي يمكن أن يظهر سريريًا وكهروفيزيولوجيًا - غالبًا ما يكشف تخطيط القلب الكهربائي مع أمراض القلب الشديدة عن مجمع QRS الواسع (> 0.12 ثانية) ، ضعف التوصيل الأذيني البطيني ، بطء القلب الجيبي (< 50) или синоатриальные паузы, удлиненный интервал QT.
يشمل علاج SS من أصل عصبي تجنب آليات الزناد لتطوير الإغماء ؛ تعديل أو إلغاء الأدوية (الأدوية الخافضة للضغط) ، إذا كانت عاملاً استفزازيًا ؛ في حالة الاكتئاب القلبي أو متلازمة الجيوب السباتية المختلطة ، يوصى بزراعة جهاز تنظيم ضربات القلب (في حالة وجود أكثر من 5 نوبات إغماء خلال العام ، في حالة الإصابات أو الحوادث الناجمة عن الإغماء ، في المرضى الذين تزيد أعمارهم عن 40 عامًا). بالنسبة للمرضى الذين يعانون من نشأة الأوعية الدموية المبهمة لـ SS ، يشار إلى التدريب مع تغيير في وضع الجسم.
عادةً ما يتطلب الإغماء الناجم عن انخفاض ضغط الدم الانتصابي تعديل الأدوية (عادةً الأدوية الخافضة للضغط).
مع عدم انتظام ضربات القلب ، يكون العلاج بالأدوية المضادة لاضطراب النظم ضروريًا. في كثير من الحالات ، يوصى بزراعة جهاز تقويم نظم القلب. مؤشرات على السرعة: إغماء متكرر متكرر من النوع التثبيطي للقلب ، مقاوم للعلاج الدوائي ويقلل بشكل كبير من جودة حياة المرضى.
يعتبر الرجفان الأذيني من أكثر حالات عدم انتظام ضربات القلب أهمية. يؤدي عدم انتظام ضربات القلب هذا إلى مضاعفة خطر الموت الكلي والموت القلبي. من بين الآثار الضارة للرجفان الأذيني ، فإن أحد أخطرها هو الاحتمال الكبير لمضاعفات الانصمام الخثاري. وفقًا لتوصيات الخبراء الأوروبيين والأمريكيين ، فإن الأهداف الاستراتيجية للمرضى المصابين بالرجفان الأذيني الانتيابي هي استعادة إيقاع الجيوب الأنفية والحفاظ عليها بالأدوية المضادة لاضطراب النظم. مع الشكل المستقر ، من الممكن استعادة إيقاع الجيوب الأنفية بمساعدة تقويم نظم القلب أو الأدوية ، وإبطاء معدل ضربات القلب مع العلاج المتزامن المضاد للتخثر. يتضمن الشكل الدائم للرجفان الأذيني الحفاظ على الرجفان ، والتحكم في الاستجابة البطينية باستخدام العلاج المناسب المضاد للتخثر ، لذلك ، في الرجفان الأذيني ، فإن العلاج المضاد للصفيحات مهم جدًا ، وقد أصبحت معاييره أسبرين وبلافيكس ، وكذلك العلاج المضاد للتخثر - غالبًا ما يكون الدواء المفضل هو LMWH Clexane. يعتمد اختيار العلاج الأمثل للرجفان الأذيني على الضرر البنيوي للقلب ، وحالة ديناميكا الدم ، ومعدل ضربات القلب ، وخطر الانصمام الخثاري وعوامل أخرى.
يرجع سبب الإغماء المصاحب لانخفاض النتاج القلبي إلى أمراض انسداد القلب والأوعية الدموية ، لذا فإن علاج هذه السير الذاتية يتحدد بالمرض الأساسي.
وبالتالي ، يمكن أن تكون SS علامة على عدد كبير من الأمراض المختلفة ، بما في ذلك الأمراض الخطيرة للغاية. لن يؤدي تشخيصهم في الوقت المناسب والعلاج الموصوف بشكل صحيح إلى تحسين نوعية حياة المريض بشكل كبير فحسب ، بل سيؤدي أيضًا إلى تحسين التشخيص الإضافي.
تمت مناقشة عدم انتظام ضربات القلب البطيني الحاد ومتلازمة ما بعد الإنعاش (PSS) من قبل موظف في قسم الإنعاش والعناية المركزة في معهد أمراض القلب المسمى باسم N.N. اختصار الثاني. Strazhesko من أكاديمية العلوم الطبية في أوكرانيا ، دكتور في العلوم الطبية Oleg Igorevich Irkin.
- يعكس عدم الاستقرار الكهربائي لعضلة القلب قابليتها للتأثر بتطور عدم انتظام ضربات القلب الذي يهدد الحياة (الرجفان البطيني وتسرع القلب البطيني المستمر) عند تطبيق منبهات خارجية لقوة العتبة (B. Lown ، 1984). تم تحديد مكونات عدم الاستقرار الكهربائي في عام 1987 بواسطة P. Coumel:
- الركيزة المولدة لعدم انتظام ضربات القلب (مستمرة ، غير مستقرة) ؛
- عوامل استفزازية (عدم توازن الكهارل ، كاتيكولاميني الدم ، الأدوية) ؛
- المحفزات (انقباض البطين ، نقص تروية عضلة القلب).
تظهر الدراسات الفيزيولوجية الكهربية أنه لوحظ عدم استقرار عضلة القلب الكهربائية في المرضى الذين يعانون من SS بعد احتشاء عضلة القلب ، لذلك يواجه الممارسون مشكلة مهمة - لتقليل خطر وفاة المرضى بسبب عدم استقرار عضلة القلب الكهربائي.
في عام 1993 ، أظهر K. Teo (JAMA) التأثير الوقائي للعديد من الأدوية المضادة لاضطراب النظم في MI. تقريبًا جميع فئات الأدوية المضادة لاضطراب النظم المستخدمة على نطاق واسع في الممارسة السريرية تزيد من خطر الوفاة لدى المرضى. الاستثناءات من هذه هي حاصرات ب ، وكذلك الأميودارون. في نفس العام ، نشر هيلد ويوسف نتائج دراسة تبحث في تأثير الاستخدام طويل الأمد لمثبطات البيتا بعد احتشاء عضلة القلب الحاد على المخاطر المحتملة للوفاة لدى المرضى. اتضح أن B-blockers مقارنة مع الدواء الوهمي يقلل بشكل كبير من خطر جميع الوفيات بنسبة 23٪ ، والموت المفاجئ بنسبة 32٪ ، والوفيات الأخرى بنسبة 5٪.
لم تؤد الدراسات حول تأثير الأدوية الأخرى المضادة لاضطراب النظم على مخاطر الوفاة وأحداث الشريان التاجي لدى المرضى إلى نتائج مريحة. أظهر Encainide / flecainide (الفئة الأولى) في دراسة CAST-1 (Echt et al. ، 1991) انخفاضًا في عدد المرضى بدون أحداث تاجية مقارنة مع الدواء الوهمي. تم الحصول على نتائج مماثلة في دراسة د-سوتالول (الفئة الثالثة) في عام 1996 (SWORD ، والدو وآخرون) ، عندما كان معدل الوفيات الإجمالي ، والوفيات القلبية وعدم انتظام ضربات القلب أقل بشكل ملحوظ في مجموعة الدواء الوهمي. في دراسة DIAMOND-MI (Kober et al. ، 2000) ، أظهر dofetilide انخفاضًا غير معتد به في إجمالي الوفيات الناجمة عن أمراض القلب وعدم انتظام ضربات القلب ، مع زيادة طفيفة في حدوث HF مقارنة مع الدواء الوهمي.
قارنت دراسة SSSD (دراسة إسبانية عن الموت المفاجئ) مثيرة للاهتمام مع متابعة لمدة 2.8 سنة بين عقارين مختلفين من الأدوية المضادة لاضطراب النظم. اشتملت الدراسة على 368 مريضًا لديهم تاريخ من احتشاء عضلة القلب ، وانخفاض الكسر القذفي للبطين الأيسر ، والانقباضات البطينية المعقدة. تم إجراء العلاج باستخدام الأميودارون في مجموعة واحدة والميتوبرولول في مجموعة أخرى. أظهرت النتائج في مجموعة الأميودارون أن معدل الوفيات الناتج عن عدم انتظام ضربات القلب كان أقل بكثير من مجموعة الميتوبرولول (3.5 مقابل 15.4٪ على التوالي). في الدراسات اللاحقة (EMIAT ، CAMIAT) ، أظهر الأميودارون أيضًا بقاء أفضل للمريض وخطرًا أقل للموت الناتج عن عدم انتظام ضربات القلب.
في عام 1997 ، أكد التحليل التلوي للدراسات التي أجريت على الأميودارون في احتشاء عضلة القلب الحاد (5101 مريضًا) وفشل القلب (1452 مريضًا) مرة أخرى أن استخدام الأميودارون يقلل بشكل كبير من الوفيات الإجمالية وعدم انتظام ضربات القلب والمفاجئة مقارنة مع الدواء الوهمي.
كما وجد أن فعالية الأميودارون تعتمد على معدل ضربات القلب. في دراسة EMIAT (Fance et al. ، 1998) ، عند تناول الأميودارون بمستوى أساسي يزيد عن 84 نبضة / دقيقة ، كان خطر حدوث اضطرابات النظم 54٪ ، ومع معدل ضربات قلب أساسي أقل من 63 نبضة / دقيقة. - 17٪ فقط. أظهرت دراسة ECMA (Boutitue et al. ، 1999) أنه عندما يتباطأ معدل ضربات القلب إلى أكثر من 80 نبضة في الدقيقة ، فإن خطر حدوث اضطرابات النظم أثناء تناول الأميودارون هو 59٪ ، بينما عند التباطؤ إلى أقل من 65 نبضة. في الدقيقة - 12٪.
في عام 1999 ، تم نشر نتائج دراسة ARREST (الأميودارون في الإنعاش المجتمعي لتسرع القلب البطيني المستدام المقاومة للحرارة ، Kudenchuk وآخرون) ، والتي قيمت فعالية الأميودارون في نظام الإنعاش القياسي. تضمنت خوارزمية الإجراءات في حالة الرجفان البطيني (VF) أو تسرع القلب البطيني (VT) الإنعاش القلبي الرئوي (CPR) قبل توصيل شاشة تخطيط القلب ، في وجود VF / VT على الشاشة: ثلاث صدمات متتالية لمزيل الرجفان مع زيادة الطاقة ، في حالة استمرار أو تكرار الإنعاش القلبي الرئوي المستمر VF / VT ، تم إجراء التنبيب الرغامي ، وتم ثقب الوريد ، وتم حقن الإبينفرين (1 مجم كل 3-5 دقائق). تم استكمال التفريغ المتكرر لمزيل الرجفان وإدخال مضادات اضطراب النظم الوريدي (ليدوكائين ، بريتيليوم ، بروكاييناميد) بأميودارون (300 مجم) أو دواء وهمي. كانت مدة الإنعاش هي نفسها تقريبًا في كلتا المجموعتين ، ولكن كان عدد تصريفات مزيل الرجفان في مجموعة الدواء الوهمي أكبر (6 ± 5 مقابل 4 ± 3 في مجموعة الأميودارون) ، وعدد المرضى الذين نجوا حتى وقت الاستشفاء في المجموعة أ.